La importancia de la gestión de riesgos en la validación de software GxP
Introducción
En la industria regulada, como la farmacéutica, dispositivos médicos y biotecnológica, la validación de software GxP es un proceso para garantizar que los sistemas informáticos utilizados en la gestión de datos críticos cumplan con los más altos estándares de calidad, seguridad e integridad.
En este contexto, la validación de software GxP no solo implica probar su funcionalidad, sino también evaluar los riesgos asociados con su implementación y uso, asegurando que se minimicen las probabilidades de fallos que podrían comprometer la integridad de los datos o la seguridad del paciente. Una estrategia sólida de gestión de riesgos permite a las empresas reguladas identificar, evaluar y mitigar posibles amenazas antes de que se conviertan en problemas críticos.
El objetivo de este artículo es proporcionar una visión detallada sobre la importancia de la gestión de riesgos en la validación de software GxP, destacando los beneficios de su aplicación, los requisitos normativos involucrados y las mejores prácticas para garantizar el cumplimiento de las regulaciones vigentes.
⚠️¿Qué es la Gestión de Riesgos en la Validación de Software GxP?
La gestión de riesgos es un proceso sistemático que permite identificar, analizar y mitigar posibles problemas que podrían afectar la calidad, seguridad o integridad de un sistema computarizado. En el ámbito de la validación de software GxP, este enfoque se centra en minimizar los riesgos que puedan comprometer la funcionalidad del software, la precisión de los datos o el cumplimiento regulatorio.
Dentro de los entornos GxP, la validación de software es un requisito para garantizar que los sistemas cumplen con los estándares de calidad y seguridad exigidos por las autoridades reguladoras. La gestión de riesgos complementa este proceso al proporcionar una metodología estructurada para evaluar la criticidad de cada componente del software y enfocar los esfuerzos en las áreas que representan un mayor impacto para la calidad del producto o la seguridad del paciente.

Las normativas y estándares clave que regulan la gestión de riesgos en la validación de software GxP incluyen:
La combinación de estas regulaciones con un enfoque sólido de gestión de riesgos permite a las empresas garantizar que sus sistemas cumplan con las expectativas de las agencias regulatorias y operen de manera segura y confiable.
✅Beneficios de la Gestión de Riesgos en la Validación de Software GxP
La gestión de riesgos desempeña un papel fundamental en la validación de software GxP, ya que permite poner en perspectiva (desde diferentes ángulos) la probabilidad de errores que puedan comprometer la calidad del producto o la seguridad del paciente. A continuación, enlistamos algunos beneficios que aporta la gestión de riesgos en la validación de software GxP y cómo su correcta implementación puede mejorar la fiabilidad y seguridad de estos sistemas:
Cumplimiento Regulatorio
Uno de los principales beneficios de la gestión de riesgos en la validación de software GxP es facilitar el cumplimiento normativo. Los organismos reguladores, como la FDA y la EMA, exigen que las empresas garanticen la seguridad y confiabilidad de los sistemas utilizados en el desarrollo y fabricación de productos regulados.
La gestión de riesgos permite documentar y justificar decisiones clave dentro del proceso de validación, asegurando que se cumplan las expectativas regulatorias. Además, facilita auditorías, ya que proporciona un enfoque estructurado para evaluar y mitigar posibles problemas, lo que reduce el riesgo de no conformidades y sanciones regulatorias.
Optimización del Proceso de Validación
Un enfoque basado en riesgos permite optimizar la validación al centrar los esfuerzos en las áreas de mayor impacto. En lugar de aplicar una validación exhaustiva y uniforme a todos los elementos del sistema, la gestión de riesgos ayuda a priorizar las funciones críticas, reduciendo la carga de trabajo en aspectos de menor importancia.
Este enfoque no solo aumenta la eficiencia, sino que también reduce costos y tiempos de validación. Al enfocarse en los puntos clave, las empresas pueden liberar recursos para otras actividades estratégicas sin comprometer la calidad del proceso de validación.
Reducción de Riesgos Operacionales
Los sistemas en entornos GxP manejan datos importantes para la producción, control de calidad y cumplimiento normativo. Un fallo en estos sistemas puede generar consecuencias graves, como datos incorrectos y pérdida de información clave que derivará en incumplimiento regulatorio y una potencial consecuencia negativa para el paciente.
La gestión de riesgos ayuda a identificar y mitigar estos posibles problemas antes de que ocurran. Implementar controles adecuados, reduce significativamente la probabilidad de errores operacionales y sus consecuencias.
Garantía de la Integridad de los Datos
En entornos GxP, cualquier alteración, pérdida o falsificación puede comprometer la validez de los resultados y la seguridad del producto final, por lo que la integridad de los datos es fundamental. La gestión de riesgos ayuda a evaluar la vulnerabilidad de los datos y a implementar medidas para prevenir, detectar y corregir posibles alteraciones.
Las estrategias para garantizar la integridad de los datos incluyen el uso de controles de acceso, registros de auditoría inmutables y procedimientos de respaldo de información. Estos mecanismos aseguran que los datos almacenados en sistemas validados sean confiables, rastreables y estén protegidos contra manipulaciones no autorizadas.

🛠️Metodologías y Herramientas para la Gestión de Riesgos
Existen diversas metodologías utilizadas en la gestión de riesgos dentro de la validación de sistemas GxP, cada una con enfoques específicos para identificar, evaluar y mitigar posibles fallos.
Una de las metodologías más utilizadas es FMEA (Failure Modes and Effects Analysis), que permite analizar los posibles modos de fallo de un sistema, evaluar sus efectos y establecer medidas preventivas para minimizar su impacto. Esta técnica ayuda a priorizar los riesgos según su gravedad, frecuencia de ocurrencia y detectabilidad, lo que facilita la toma de decisiones en la validación del software.
Otra metodología clave es HACCP (Hazard Analysis and Critical Control Points), ampliamente utilizada en la industria alimentaria y farmacéutica, que se centra en la identificación de puntos críticos de control dentro de un proceso para prevenir riesgos antes de que ocurran. Adaptada a la validación de sistemas GxP, esta metodología permite establecer controles en fases clave del ciclo de vida del software para garantizar su confiabilidad.
Por otra parte, la ISO 31000 proporciona un marco genérico para la gestión de riesgos, aplicable a cualquier sector, incluyendo la validación de software en entornos GxP. Esta norma internacional establece principios y directrices para identificar, evaluar y tratar riesgos de manera estructurada y basada en la mejora continua.
Dentro de la industria regulada, el GAMP 5 (Good Automated Manufacturing Practice) es otro de los marcos más relevantes, ya que promueve un enfoque basado en riesgos para la validación de sistemas computarizados. GAMP 5 clasifica los sistemas según su criticidad y nivel de complejidad, permitiendo a las empresas asignar recursos de manera eficiente y enfocarse en los aspectos más críticos para el cumplimiento normativo.
Además de estas metodologías, el uso de software especializado para la gestión de riesgos en la validación GxP se ha vuelto cada vez más común.
Identificación y Evaluación de Riesgos
El primer paso en la gestión de riesgos es la identificación de amenazas potenciales que puedan afectar la funcionalidad, integridad de los datos o cumplimiento normativo del software. Una vez identificados los riesgos, es necesario categorizarlos en función de su impacto y probabilidad. Los riesgos de alto impacto, como fallos en la seguridad de los datos o errores que puedan comprometer la salud del paciente, deben recibir mayor atención. Para este propósito, se pueden emplear matrices de riesgo que clasifican las amenazas en niveles bajo, medio y alto, lo que permite enfocar los esfuerzos en las áreas más críticas.

Estrategias de Mitigación y Control de Riesgos

Después de evaluar los riesgos, se deben implementar estrategias para mitigarlos o eliminarlos. Las medidas preventivas pueden incluir controles de acceso, pruebas automatizadas, procedimientos de respaldo de datos y auditorías periódicas.
También es esencial establecer planes de contingencia para responder eficazmente ante eventos inesperados, minimizando su impacto en la operación y el cumplimiento normativo. Algunas empresas han logrado reducir significativamente los riesgos en la validación de software mediante la implementación de entornos de prueba controlados, donde se simulan escenarios de fallo antes de la implementación en producción.
Monitoreo y Mejora Continua
La gestión de riesgos no es un proceso estático; requiere una revisión y actualización constante para adaptarse a cambios regulatorios, avances tecnológicos y nuevos desafíos operacionales. Es recomendable realizar auditorías internas periódicas para evaluar la efectividad de las estrategias de mitigación y ajustar los controles según sea necesario.
El seguimiento del desempeño del sistema validado a lo largo del tiempo permite identificar oportunidades de mejora y fortalecer la estrategia de gestión de riesgos. Para ello, el uso de herramientas de monitoreo automatizado y reportes en tiempo real facilita la detección temprana de problemas y garantiza la toma de decisiones basadas en datos.
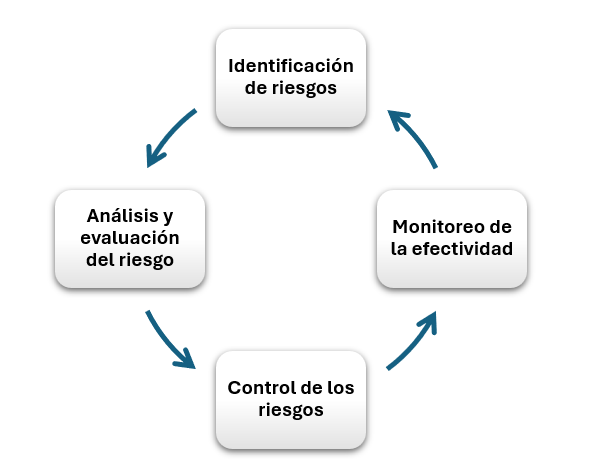
La gestión de riesgos es un ciclo sistemático de evaluación, control, comunicación y revisión periódica de los riesgos. Es un proceso que se repite a lo largo de todas las etapas del ciclo de vida de los sistemas. Adoptar este marco de trabajo permite a las empresas tomar decisiones informadas para asegurar consistencia de su aplicación en todas las funcionalidades del sistema con impacto GxP.
🧠Conclusión
La gestión de riesgos es un pilar fundamental en la validación de software GxP, ya que permite garantizar la seguridad, calidad e integridad de los datos en entornos regulados. Al aplicar metodologías estructuradas como FMEA, HACCP o GAMP 5, las empresas pueden minimizar los riesgos asociados con la implementación y operación de sistemas computarizados, asegurando el cumplimiento normativo y la eficiencia operativa.
Para mejorar su estrategia de validación, las organizaciones deben adoptar un enfoque basado en riesgos, priorizar áreas críticas y establecer controles efectivos que reduzcan la posibilidad de fallos. Además, la implementación de software especializado para la gestión de riesgos puede optimizar el proceso y facilitar auditorías regulatorias.
En un entorno en constante evolución, la flexibilidad y la mejora continua son claves para mantener la conformidad con las regulaciones vigentes y garantizar la seguridad de los productos y datos manejados por los sistemas validados.
Preguntas Frecuentes (FAQs)
¿Tienes dudas? Consulta nuestras preguntas frecuentes o contáctanos directamente.
Los principales desafíos incluyen la identificación precisa de riesgos críticos a través del conocimiento de los procesos y de la visión de los usuarios, la gestión eficiente de recursos para la validación, la adaptación a cambios regulatorios y la implementación de controles efectivos sin afectar la operatividad del software.
La validación de software se centra en asegurar que un sistema cumple con sus requisitos específicos y funciona correctamente dentro de un entorno regulado, mientras que la verificación se enfoca en comprobar que cada componente del software ha sido desarrollado de acuerdo con las especificaciones establecidas.
Una gestión de riesgos efectiva optimiza procesos, reduce costos de validación, minimiza fallos operacionales y permite una adaptación ágil a cambios regulatorios, mejorando la eficiencia y competitividad de la empresa.
